MENÜ
CH | CHF
CH | CHF
-
- Alle Zentrifugen
- Tischzentrifugen
- Standzentrifugen
- Kühlzentrifugen
- Mikrozentrifugen
- Mehrzweckzentrifugen
- Hochgeschwindigkeitszentrifugen
- Ultrazentrifugen
- Concentrator
- IVD-Produkte
- Verbrauchsartikel für Hochgeschwindigkeits- und Ultrazentrifugen
- Zentrifugenröhrchen
- Zentrifugenplatten
- Gerätemanagement-Software
- Proben- und Informationsmanagement
-
- Alle Pipetten, Dispenser und automatischen Liquid-Handling-Systeme
- Mechanische Pipetten
- Elektronische Pipetten
- Mehrkanalpipetten
- Direktverdrängerpipetten und Dispenser
- Pipettenspitzen
- Flaschendispenser
- Pipettierhilfen
- Zubehör für Dispenser und Pipetten
- Automatisches Pipettieren
- Verbrauchsartikel für die Automation
- Zubehör für die Automation
- Services für Liquid-Handling-Geräte und Pipetten
Sorry, we couldn't find anything on our website containing your search term.
Sorry, we couldn't find anything on our website containing your search term.

Schüttelkolben – viel mehr als nur zum Abfüllen von Proben
Ines Hartmann Lab Academy
- Cell Biology
- Cell Culture
- Mixers & Shakers
- Essay
Schüttelkulturen werden in Spezialgefäßen kultiviert, welche auch als Erlenmeyerkolben bekannt sind. Im Unterschied zu anderen Laborgefäßen sind Schüttelkolben so geformt, dass sie ohne Spritz- oder Verschüttungsgefahr geschüttelt werden können. Erfahren Sie mehr über Unterschiede beim Design und Material und deren Einfluss auf die Belüftung.
Geschüttelte Bioreaktoren, auch Erlenmeyer- oder einfach Schüttelkolben genannt, wurden zu Beginn des vorigen Jahrhunderts eingeführt. Mit Kapazitäten von 25 mL bis 5 Liter sind sie vielseitig für unterschiedlichste Versuchszwecke einsetzbar – von Screening und Expansion bis hin zu Mediendesign und Entwicklungsprozessen im Anfangsstadium. Schüttelkolben sind preisgünstig und eignen sich für die Kultivierung von Bakterien, Hefe, Pilzen sowie von Pflanzenzellen und tierischen Zellen in Suspension. Die Handhabung von Schüttelkolben erfordert keine spezielle Schulung. Für eine effiziente Kultivierung gilt es jedoch einiges zu beachten. Zudem gibt es verschiedene Gefäßtypen, die sich jeweils für andere Anwendungen eignen.
Kolbenmaterial – Glas versus Kunststoff
Die Kolben sind entweder aus Glas oder Kunststoff erhältlich. Für klassische Anwendungen in der Mikrobiologie sind meist wiederverwendbare autoklavierbare Erlenmeyerkolben aus Glas geeignet. Auch wenn der Sauerstoffeintrag kritisch ist, kann es vorteilhaft sein, mit Glas zu arbeiten, da Glas als hydrophiles Material die Bildung des Flüssigkeitsfilms unterstützt, der für den Sauerstoffeintrag benötigt wird. Im Vergleich dazu ist Kunststoff, sofern er nicht speziell behandelt ist, hydrophob [1]. Kommt es auf die Vermeidung von Kontaminationen an, z. B. bei empfindlichen Kulturen oder Produktionsschritten, dann bieten sterile Einwegkolben mit belüfteten Deckeln (Filter 0,2 µm) ein Höchstmaß an Komfort und Sicherheit. Es sind verschiedene Kunststoffe auf dem Markt, aus denen je nach Anwendung und persönlichen Vorlieben gewählt werden kann: von hochbeständigem Polypropylen (PP) für mikrobiologische Anwendungen bis hin zu optisch klaren Materialien insbesondere für Anwendungen in der Säugetier-Zellkultur, wie z. B. Polycarbonat (PC) oder Polyethylenterephthalat-Glycol (PETG).
Kolbendesign – Sonderformen und Schikanen
Kulturen werden geschüttelt, um die Belüftung und Nährstoffverfügbarkeit zu erhöhen sowie Sedimentation zu verhindern. Typische Erlenmeyerkolben sind kegelförmig mit einem breiteren Boden und zylindrischen Hals. Es gibt verschiedene Kolbendesigns: weit- oder enghalsig, mit oder ohne Schikanen. Zudem sind Sonderformen für einen noch besseren Gasaustausch erhältlich, z. B. der großvolumige Fernbachkolben, der über einen noch breiteren Boden und damit eine größere Fläche für den Sauerstoffeintrag verfügt, oder die Verbrauchsartikel Ultra Yield™ und Optimum Growth Flasks™, deren Form zur Maximierung des Oberflächen-Volumen-Verhältnisses optimiert wurde [2].
Mit oder ohne Schikanen: In Kolben ohne Schikanen wird eine gleichförmige und gleichmäßige Verwirbelung der Flüssigkeit mit einer klar definierten und vorhersagbaren Geometrie erzeugt [2]. In Kolben mit Schikanen wird dieser Wirbel absichtlich durch definierte Vorsprünge im Boden unterbrochen. Dieses „wirbelbrechende“ Design verbessert die Belüftung der Kultur und kann von Vorteil sein, wenn die Kultur viel Sauerstoff benötigt. Neben der besseren Belüftung können Schikane-Kolben auch bei der Handhabung viskoser Kulturen wie z. B. filamentöser Pilze sinnvoll sein, um eine Aggregation von Sporen oder eine Pelletierung der Kultur zu verhindern [3]. Andererseits ist hier die Gefahr höher, dass sich Schaum bildet, welcher den Sauerstoffeintrag behindern kann. Zudem liefern Schikane-Kolben aufgrund der abrupten Unterbrechung des Wirbels und des chaotischeren Fließverhaltens wesentlich variablere Ergebnisse als Kolben ohne Schikanen [2].
Kolbenmaterial – Glas versus Kunststoff
Die Kolben sind entweder aus Glas oder Kunststoff erhältlich. Für klassische Anwendungen in der Mikrobiologie sind meist wiederverwendbare autoklavierbare Erlenmeyerkolben aus Glas geeignet. Auch wenn der Sauerstoffeintrag kritisch ist, kann es vorteilhaft sein, mit Glas zu arbeiten, da Glas als hydrophiles Material die Bildung des Flüssigkeitsfilms unterstützt, der für den Sauerstoffeintrag benötigt wird. Im Vergleich dazu ist Kunststoff, sofern er nicht speziell behandelt ist, hydrophob [1]. Kommt es auf die Vermeidung von Kontaminationen an, z. B. bei empfindlichen Kulturen oder Produktionsschritten, dann bieten sterile Einwegkolben mit belüfteten Deckeln (Filter 0,2 µm) ein Höchstmaß an Komfort und Sicherheit. Es sind verschiedene Kunststoffe auf dem Markt, aus denen je nach Anwendung und persönlichen Vorlieben gewählt werden kann: von hochbeständigem Polypropylen (PP) für mikrobiologische Anwendungen bis hin zu optisch klaren Materialien insbesondere für Anwendungen in der Säugetier-Zellkultur, wie z. B. Polycarbonat (PC) oder Polyethylenterephthalat-Glycol (PETG).
Kolbendesign – Sonderformen und Schikanen
Kulturen werden geschüttelt, um die Belüftung und Nährstoffverfügbarkeit zu erhöhen sowie Sedimentation zu verhindern. Typische Erlenmeyerkolben sind kegelförmig mit einem breiteren Boden und zylindrischen Hals. Es gibt verschiedene Kolbendesigns: weit- oder enghalsig, mit oder ohne Schikanen. Zudem sind Sonderformen für einen noch besseren Gasaustausch erhältlich, z. B. der großvolumige Fernbachkolben, der über einen noch breiteren Boden und damit eine größere Fläche für den Sauerstoffeintrag verfügt, oder die Verbrauchsartikel Ultra Yield™ und Optimum Growth Flasks™, deren Form zur Maximierung des Oberflächen-Volumen-Verhältnisses optimiert wurde [2].
Mit oder ohne Schikanen: In Kolben ohne Schikanen wird eine gleichförmige und gleichmäßige Verwirbelung der Flüssigkeit mit einer klar definierten und vorhersagbaren Geometrie erzeugt [2]. In Kolben mit Schikanen wird dieser Wirbel absichtlich durch definierte Vorsprünge im Boden unterbrochen. Dieses „wirbelbrechende“ Design verbessert die Belüftung der Kultur und kann von Vorteil sein, wenn die Kultur viel Sauerstoff benötigt. Neben der besseren Belüftung können Schikane-Kolben auch bei der Handhabung viskoser Kulturen wie z. B. filamentöser Pilze sinnvoll sein, um eine Aggregation von Sporen oder eine Pelletierung der Kultur zu verhindern [3]. Andererseits ist hier die Gefahr höher, dass sich Schaum bildet, welcher den Sauerstoffeintrag behindern kann. Zudem liefern Schikane-Kolben aufgrund der abrupten Unterbrechung des Wirbels und des chaotischeren Fließverhaltens wesentlich variablere Ergebnisse als Kolben ohne Schikanen [2].
Mehr erfahren
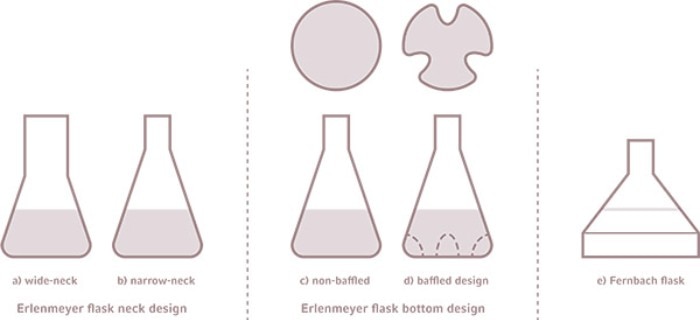
Erlenmeyerkolben-Designs (a) weithalsig (b) enghalsig (c) ohne Schikanen (d) mit Schikanen (e) Fernbachkolben
https://handling-solutions.eppendorf.com/cell-handling/bioprocess/processes-and-applications/detailview/news/its-not-just-about-size-talking-about-shake-flasks-and-bioreactors/
Kolbenverschlüsse – von herkömmlicher Baumwolle zu belüfteten Deckeln.
Um eine Kontamination der Kulturen zu verhindern, sind diverse Kolbenverschlüsse erhältlich. Der Verschluss soll Kontaminationen verhindern, muss aber auch für eine ausreichende Belüftung der Kulturen sorgen. Die Auswahl reicht von herkömmlichen Stopfen über Metalldeckel und Silikonschwämme bis hin zu Einweg-Filterdeckeln. Die Sauerstoffeintragsrate durch den Verschluss hängt vom Diffusionskoeffizienten für Sauerstoff in dem Material, der Breite der Halsöffnung und der Tiefe des Stopfens ab [1]. Ist Kontamination ein Problem, dann sollten Baumwollstopfen vermieden werden. Baumwolle kann durch Spritzer (z. B. bei Verwendung von Schikane-Kolben) oder Kondensatbildung feucht werden, was zu einer Kreuzkontamination führen kann. Generell sollte darauf geachtet werden, den Kolbenverschluss nicht feucht werden zu lassen – nicht nur um Kreuzkontaminationen zu reduzieren, sondern auch um die Gasdurchlässigkeit nicht zu verringern. Das gilt auch für nicht hydrophobe Filtermaterialien, welche ebenfalls Flüssigkeit aufsaugen können. Für parallele Versuche sollten gleichartige Verschlüsse gewählt werden, um Differenzen bei den Gasaustauschraten zu vermeiden.
Welche Füllvolumen werden empfohlen?
Je mehr die Kultur belüftet werden muss, desto kleiner sollte das gewählte Füllvolumen sein. Als Faustregel sollte bei mikrobiellen Kulturen 1/5 der Nennkapazität des Kolbens, z. B. 100 mL bei einem 500-mL-Erlenmeyerkolben, nicht überschritten werden. Wird ein maximaler Sauerstoffeintrag benötigt, z. B. für lange Fermentationen von Stämmen mit hoher Sauerstoffzehrung, dann sollte das Füllvolumen sogar auf ganze 10 % verringert und die Drehzahl so stark erhöht werden, wie es die Scherfestigkeit der Kultur erlaubt. Bei schersensitiven Säugetierzellkulturen sind höhere Füllvolumen zwischen 30 und 40 % bei niedrigeren Schüttelgeschwindigkeiten von ≤ 150 rpm üblich. In den letzten Jahren wurden spezifische Kolbentypen für die Protein- oder Plasmidexpression mit hoher Ausbeute entwickelt, so z. B. die oben genannten Ultra Yield™ und Optimum Growth Flasks™. Diese weisen ein optimiertes Oberflächen-Volumen-Verhältnis und Bodenschikanen für einen verbesserten Sauerstoffeintrag auf, was höhere Füllvolumen erlaubt [2].
Literatur:
[1] Pauline M. Doran, Bioprocess Engineering Principles (Second Edition), Chapter 10 - Mass Transfer, 2013
[2] htslabs.com
[3] J. Büchs / Biochemical Engineering Journal 7 (2001) 91–98
[4] Filamentous Fungal Cultures – Process Characteristics, Products, and Applications Hesham A. El-Enshasy, in Bioprocessing for Value-Added Products from Renewable Resources, 2007
Kolbenverschlüsse – von herkömmlicher Baumwolle zu belüfteten Deckeln.
Um eine Kontamination der Kulturen zu verhindern, sind diverse Kolbenverschlüsse erhältlich. Der Verschluss soll Kontaminationen verhindern, muss aber auch für eine ausreichende Belüftung der Kulturen sorgen. Die Auswahl reicht von herkömmlichen Stopfen über Metalldeckel und Silikonschwämme bis hin zu Einweg-Filterdeckeln. Die Sauerstoffeintragsrate durch den Verschluss hängt vom Diffusionskoeffizienten für Sauerstoff in dem Material, der Breite der Halsöffnung und der Tiefe des Stopfens ab [1]. Ist Kontamination ein Problem, dann sollten Baumwollstopfen vermieden werden. Baumwolle kann durch Spritzer (z. B. bei Verwendung von Schikane-Kolben) oder Kondensatbildung feucht werden, was zu einer Kreuzkontamination führen kann. Generell sollte darauf geachtet werden, den Kolbenverschluss nicht feucht werden zu lassen – nicht nur um Kreuzkontaminationen zu reduzieren, sondern auch um die Gasdurchlässigkeit nicht zu verringern. Das gilt auch für nicht hydrophobe Filtermaterialien, welche ebenfalls Flüssigkeit aufsaugen können. Für parallele Versuche sollten gleichartige Verschlüsse gewählt werden, um Differenzen bei den Gasaustauschraten zu vermeiden.
Welche Füllvolumen werden empfohlen?
Je mehr die Kultur belüftet werden muss, desto kleiner sollte das gewählte Füllvolumen sein. Als Faustregel sollte bei mikrobiellen Kulturen 1/5 der Nennkapazität des Kolbens, z. B. 100 mL bei einem 500-mL-Erlenmeyerkolben, nicht überschritten werden. Wird ein maximaler Sauerstoffeintrag benötigt, z. B. für lange Fermentationen von Stämmen mit hoher Sauerstoffzehrung, dann sollte das Füllvolumen sogar auf ganze 10 % verringert und die Drehzahl so stark erhöht werden, wie es die Scherfestigkeit der Kultur erlaubt. Bei schersensitiven Säugetierzellkulturen sind höhere Füllvolumen zwischen 30 und 40 % bei niedrigeren Schüttelgeschwindigkeiten von ≤ 150 rpm üblich. In den letzten Jahren wurden spezifische Kolbentypen für die Protein- oder Plasmidexpression mit hoher Ausbeute entwickelt, so z. B. die oben genannten Ultra Yield™ und Optimum Growth Flasks™. Diese weisen ein optimiertes Oberflächen-Volumen-Verhältnis und Bodenschikanen für einen verbesserten Sauerstoffeintrag auf, was höhere Füllvolumen erlaubt [2].
Literatur:
[1] Pauline M. Doran, Bioprocess Engineering Principles (Second Edition), Chapter 10 - Mass Transfer, 2013
[2] htslabs.com
[3] J. Büchs / Biochemical Engineering Journal 7 (2001) 91–98
[4] Filamentous Fungal Cultures – Process Characteristics, Products, and Applications Hesham A. El-Enshasy, in Bioprocessing for Value-Added Products from Renewable Resources, 2007
Mehr erfahren

